식약처 식품의약품안전평가원은 OECD 승인 피부감작성 동물대체시험법의 국내 도입을 위한 가이드라인을 발간했다.
‘화장품 동물대체시험법 가이드라인’에 수록된 시험법은 인체피부각질세포에서 항산화반응인자(ARE-Nrf2)의 조절을 받는 특정 효소(루시퍼라아제)의 발현 정도를 측정함으로써 피부감작성 반응 여부를 평가하는 방법이다.
이는 UN GHS 기준에 따른 피부감작물질과 비감작물질을 구별하는데 사용하는 시험법이다. 때문에 피부감작성 독성발현경로의 두 번째 핵심 단계인 ‘각질세포의 활성화’에 대한 생체외 시험이다. 유전자의 항산화 반응요소에 의해 전사(transcription) 조절을 받는 루시퍼라아제(Luciferase) 유전자를 안정적으로 삽입한 인체 각질세포주를 사용한다. 발현 수준은 발광측정기(luminometer)를 통해 측정한다.
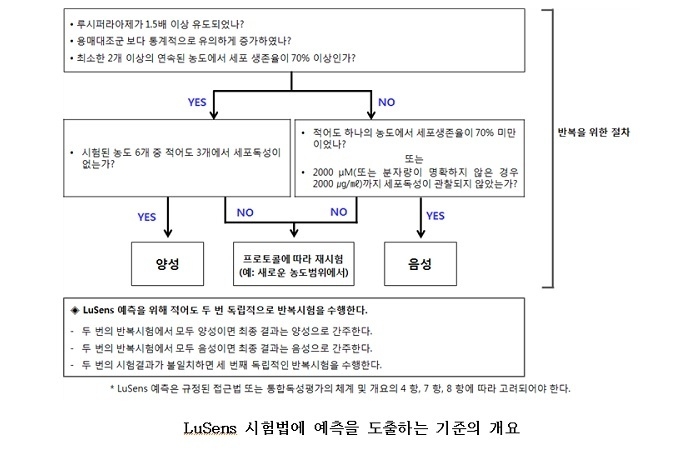
시험법은 두 단계로 이뤄진다. 첫째는 세포독성 용량을 설정하는 단계이고, 둘째는 루시퍼라아제 발현을 평가하는 단계다. 결과 판성 시 세포독성(즉 세포생존율이 70% 이상)이 없는 두 개의 연속적인 시험농도에서 용매대조군과 비교했을 때, 통계적으로 유의하게 루시퍼라아제 유도가 1.5배 이상이어야 한다. 또한 적어도 세 개의 시험 농도에서는 세포 독성이 없어야 한다.(세포 생존율은 70% 이상)
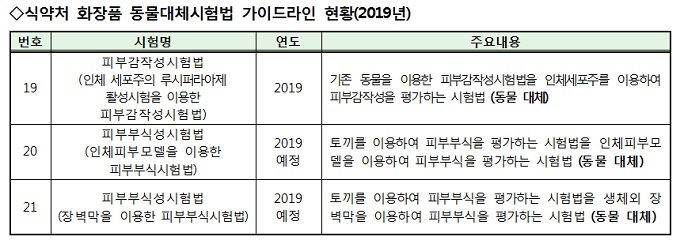
식약처는 2007년부터 화장품 안전성 평가에 필요한 동물대체시험법을 마련하고 있으며, 현재 19개 가이드라인을 제정했다. 이를 널리 알리기 위해 오는 10월, 국내 비임상시험실시기관을 비롯해 산업계와 학계를 대상으로 ‘함께하는 동물대체시험법 교육 워크숍’을 개최할 계획이다.
한편 2019년에 예정된 시험법은 ▲피부부식성시험법(인체피부모델을 이용) ▲피부부식성시험법(장벽막을 이용) 등이다.