지난 10일 장협 주최 ‘미국 화장품 규제 현대화법(MoCRA) 웨비나’는 396명이 순간 접속할 정도로 관심이 높았다. 기업별 사정에 따라, 또는 당장의 대응에 혼란을 느낀 미국향 수출 기업들의 사전 및 실시간 질의가 150여 건을 훌쩍 넘길 정도로 쏟아졌다. 이를 온전히 받아낸 FDA 전문 컨설턴트 존권 대표를 12일 ‘K-뷰티 엑스포’가 열린 킨텍스에서 만났다.

일단 비관세무역장벽이라 할만큼 미국이 MoCRA를 추진하는 이유는 뭘까? 이에 대해 존권 대표는 “MoCRA는 80여 년 만에 처음으로 연방 화장품법이 업데이트 된 것이다. 지난 10년여 의회와 FDA, 소비자 및 환경 단체, 뷰티 및 퍼스널케어 산업을 포함한 많은 이해 관계자들의 노력 끝에 MoCRA가 탄생했다. 이로써 FDA는 화장품 시장을 규제할 수 있는 더 많은 권한을 부여받았다”라며 의미를 전했다.
또한 “지난 코로나 시기 마스크, 손세정제 등 방역물품이 일시에 쏟아지면서 미국 소비자들의 불만이 모니터링 됐다. 이후 의회에서 검증 안된 제품 수입에 대해 제동을 걸고, 미국 시장에서 점유율이 높아지고 있는 외국산 화장품에 대한 자국산업 보호 등 여론이 형성됐다”고 설명했다. 그 여파로 미국 바이든 대통령이 2022년 12월 29일 화장품 규제 현대화법이 포함된 2023년 통합세출법에 서명함으로써 1년의 유예기간이 주어졌다.
존권 대표는 “포털사이트는 의견수렴일인 10월 18일 이후 10월 말 또는 11월 초 오픈할 것으로 예상된다. 현지에서도 새롭게 만들기엔 시간이 촉박해 기존 OTC의 화장품 버전(FDA Direct)으로 공개될 가능성이 크다"고 말했다.
그러다보니 당장 시설등록 및 제품 리스팅 플랫폼이 오픈도 안된 상태에서 관련 FDA가 시간에 쫓기고 있음이 드러났다. 웨비나에서 기업들의 질문은 MoCRA 추진 일정과 시설등록 및 제품리스팅, RP의 역할에 모아졌다.
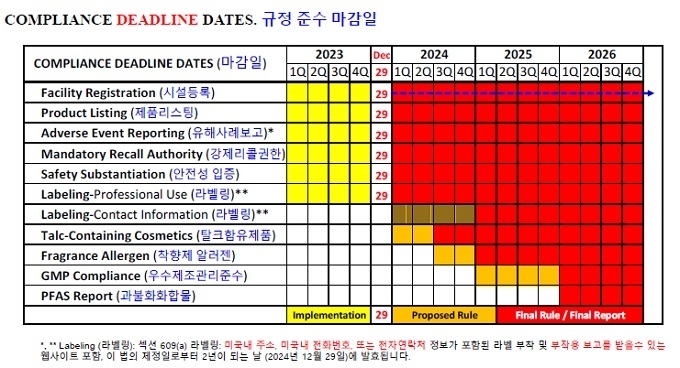
먼저 ▲ 2023년 12월 29일까지 준수해야 할 내용은 ① 시설등록(Facility Registration) ② 제품 리스팅(Product Listing) ③ 프로페셔널 제품의 라벨링(Labeling-Professional Use)) 등이다. 이어 ▲ 2024년 이후 예정된 규정은 ① 착향제 알레르기 표기(Fragrance Allergen) ② 탈크 함유제품(Talc-Containing Cosmetics) ③ 우수제조관리 준수(GMP Compliance) 등이다.
시설등록은 2년마다 등록 경신해야 한다. 기존시설은 제정일로부터 1년 이내에 등록해야 하며, 기한은 2023년 12월 29일까지다. 신규시설은 첫 제조일로부터 60일 이내 또는 기존시설 등록 마감일로부터 60일이내(두 날짜 중 더 늦은 날짜로)다.
시설등록 시 등록정보 변경 사항 (➊ 시설등록번호(FEI) ➋ 책임자명, 주소, 전화번호, 전자연락처 ➌ 미국 대리인 전화번호, 전자연락처 ➍시설에서 제조 또는 가공된 화장품 정보-화장품명(라벨 기재), 카테고리, 각 성분명(관용명 또는 일반명으로 착향제, 향 또는 색소 포함)을 60일 이내 제출해야 한다. 만일 업데이트를 제출할 필요가 없는 시설을 조유하거나 운영하는 경우 약식 등록 경신 프로세스가 제공될 예정이다.
존권 대표는 “책임자를 대신하여 시설에서 화장품을 제조 또는 가공하는 경우(위탁), 해당 시설이 자기 화장품 또는 한 명 이상의 책임자를 대신하여 제조 또는 가공하는 경우(제조사 자체 브랜드)에도 해당시설에 대해 단일 등록만 하면 된다. 즉 해당 시설 또는 해당 시설에서 제품을 제조 또는 가공하는 책임자가 등록하면 된다”고 설명했다.

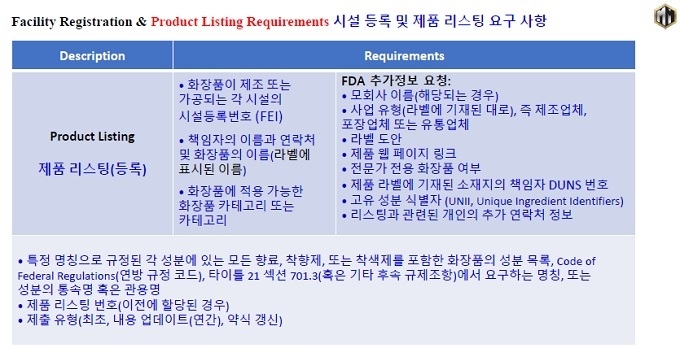
제품 리스팅은 매 1년마다 업데이트를 해야 한다. 기존 제품은 제정일로부터 1년 이내에 등록해야 하며 2023년 12월 29일이 마감 시한이다. 신규 제품이라면 처음 시판되는 미국 주(state) 간 상거래에서 시판 후 120일 이내 등록해야 한다. 제품 리스팅을 하려면 라벨에 기재된 소재지의 책임자 던즈 넘버가 필요하다. (DUNS Number는 D&B(Dun & Bradstreet)가 발급하는 국제사업자 등록번호로 기업식별코드를 말한다)
제품 리스팅 시 ➊화장품 제조 또는 가공되는 각 시설의 시설등록번호(FEI) 및 책임자의 이름과 연락처 ➋화장품 명(라벨과 일치), 화장품 카테고리 ➌사업자 유형(제조사, 포장업체, 유통업체(브랜드사) ➍라벨 도안, 제품 웹페이지 링크, 전문가전용 화장품 여부 ➎라벨에 기재된 책임자 던즈 번호 ➏고유성분 식별자(UNII) ➐리스팅과 관련된 개인의 추가 연락처 정보 등을 기재토록 하고 있다.
웨비나 참가 기업의 주요 질문 중 RP(Responsible Person) 및 소규모 기업(small Business)에 대한 질문이 많았다.
책임자란 제조사, 포장업자, 유통업자(브랜드) 중 한 업체가 된다. 책임자는 미국 내 주소와 전화번호, 전자연락처가 있는 법인이나 자연인(수입자, 유통업자, FDA U.S. Agent 또는 콜센터)을 임명하고 라벨에 기재하면 된다.
존권 대표는 “EU CPNP는 수입된 화장품에 관해서는 각각의 수입자가 자신이 시장에 출시하는 특정 화장품에 대한 책임자가 되지만, FDA는 제조사, 포장업자, 유통업자 중 하나면 된다. 책임자의 역할은 시설등록 및 제품 리스팅, 유해사례 보고 및 기록유지, 안전성 입증, 라벨링 표기, 착향제 알러젠 정보 제출, 학향제 기록 엑세스 의무 등”이라고 말했다.
소규모 기업은 섹션 606(GMP) 또는 607(등록 및 제품 리스팅)이 적용되지 않는다. 여기서의 소규모 기업은 최근 3년 동안 미국에서 화장품의 평균 연간 총 매출이 100만불 미만인 경우 해당된다. 다만 눈의 점막 접촉 화장품, 주사용 화장품, 내복용 화장품, 24시간 이상 외관 변경 화장품은 제외된다. 이와 관련 존권 대표는 "한 가지 명확하게 확인 안된 부분은 소규모 기업이 해외 기업이 아닌 미국 기업에게만 특혜가 주어질 것이라는 점이 우려된다"고 해설했다.
대한화장품협회를 통해 존권 대표는 꾸준히 미국 FDA 규정을 소개해왔다. 유튜브(대한화장품협회)에서 MoCRA 웨비나 동영상이 두 편(2023.02.14. 2023.10.10.)을 시청할 수 있다.
한편 존권 대표는 FDA 관련 다양한 카테고리 업무를 다룬 전문 컨설턴트로 LG생활건강, 한국콜마 등을 비롯 다수 기업 자문을 맡고 있다.(연락처 john@mtomglobal.com)