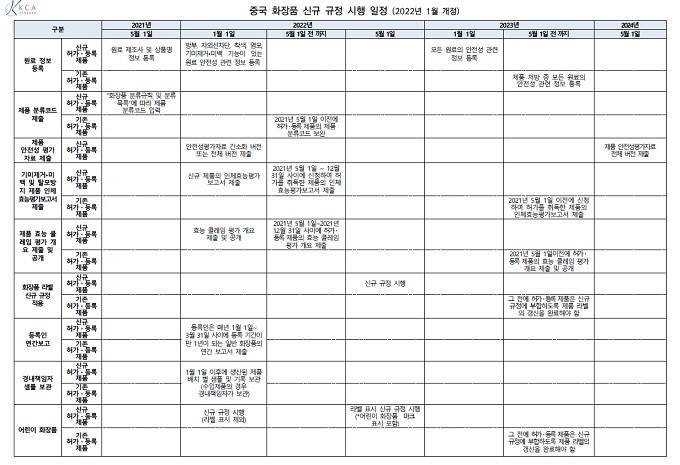
대한화장품협회는 7일 중국 화장품 신규 규정의 시행 일정을 업데이트했다. 이에 따르면 신규 또는 기존 허가·등록 제품의 경우 ▲올해 1월 1일부터 등록인은 매년 1월 1일~3월 31일 사이에 등록기간이 만 1년이 되는 일반 화장품의 연간 보고서를 체출 ▲1월 1일 이후에 생산된 제품 배치별 샘플 및 기록 보관(수입제품의 경우 경내책임자가 보관) 해야 한다.
별도로 기존 허가·등록 제품의 경우, 2022년 5월 1일 이전에 허가·등록 제품의 분류코드를 보완해야 한다. 또한 2023년 5월 1일 전까지 ①제품 처방 중 모든 원료의 안전성 관련 정보 등록 ②2021년 5월 1일 이전에 신청하여 허가를 취득한 제품의 인체효능평가보고서 제출 ③등록 제품의 효능 클레임 평가 개요 제출 및 공개 ④그전에 허가·등록 제품은 신규 규정에 부합하도록 제품 라벨의 갱신 완료 등을 해야 한다.
한편 질문이 많은 내용도 함께 공개했다. 먼저 화장품 허가·등록을 위한 품질안전책임자의 정보 및 이력서 제출에는 성명, 신원 증명서류 유형 및 번호 포함, 이력서는 관련 교육 배경, 업무 경력 및 기타 내용이 포함되어야 한다.
화장품의 제조사 위탁생산인 경우에는 품질관리체계 개요를 제출해야 한다. 허가인·등록인, 수탁생산 제조사 모두 대표자의 성명, 신원증명서류 유형 및 번호를 제출해야 한다.
원료 안전성 관련 정보의 등록 주체는 원료 생산업체이며, 실제 생산업체 또는 동일 그룹에 소속된 계열사, 원료 생산 위탁 기업이 해당한다. 경외 또는 경내 원료 생산기업은 직접 화장품 원료 안전성 정보를 보고할 수 있고, 수권자는 원료정보의 보고 및 유지보수를 진행할 수 있다.
기사용화장품원료명칭목록(2021년판)에 수록된 원료도 원료 안전성 관련 정보제출 대상에 해당된다. 화장품을 중국으로 수출하기 위해서는 제품 처방에 사용된 모든 원료가 반드시 중국에서 사용된 이력이 있는 원료여야 한다. 기사용 목록에 없는 원료는 ‘화장품 신원료 허가, 등록 자료 관리규정’에 따라 신원료 허가를 취득하거나 등록 후 사용할 수 있다. (자세한 내용은 대한화장품협회 홈페이지 참조)






























