“미국 FDA의 경고서한(Warning Letter)을 받은 제조사 제품은 통관지체(detention) 및 통관 불허(refusal)로 이어질 수 있다.” 미국 FDA 컨설턴트인 엠톰(MTOM) 존권(John Kwon) 대표의 말이다.
대체로 OTC Drug에만 허용되는 문구를 화장품 라벨링에 표기하거나, OTC 제품인데 등록을 하지 않게 되는 경우 FDA 웹사이트에 게재하여 해당 업체에 경고를 하게 된다. 회사 이름과 함께 무엇을 잘못했는지에 대한 정보가 공개된다.
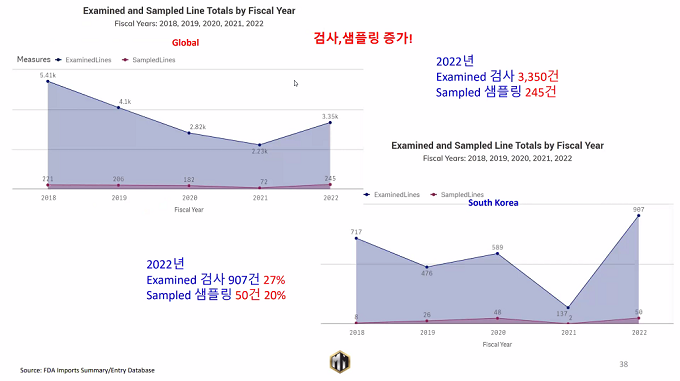
존권 대표에 따르면 최근 5년 동안 수입 거부된 한국 화장품은 480건이다. 2022년에만 전체 수입 거부 1050건 중 118건으로 거부율이 11%나 된다. 이럴 경우 경고서한을 받을 수 있다.
대한화장품협회는 최근 미국 FDA의 경고서한 사례를 분석한 자료에서 대표적인 유형 7가지를 제시했다. ① 화장품으로 판매한 제품에서 의약품의 효능효과를 클레임한 경우 ② 색소 규정 위반 ③ 미생물에 오염된 불량 화장품 ④ 의료기기로 허가를 받고 팔아야 하는데, 이를 화장품으로 판매한 경우 ⑤ 화장품 및 의약품 규정을 위반 ⑥ 안전성 및 라벨링 위반 ⑦ 의약품 GMP 미준수 등이다.
먼저 의약품에서만 허용되는 클레임을 화장품 라벨에 표기하거나 유튜브·페이스북·웹사이트·브로셔·제품 홍보자료 등에 사용할 경우다. 주로 △ acne treatment (여드름 트리트먼트) △ cellulite reduction (셀루라이트 감소) △ stretch mark reduction (스트레치 마크 감소) △wrinkle removal (주름 제거) △ dandruff treatment (비듬 트리트먼트) △ hair restoration (모발 복원) △ eyelash growth (속눈썹 성장) 등이 경고 서한(Warning letter)을 받게 된다. 이를 받았을 때는 제품 포장, 광고 문구, 웹사이트 등에 사용된 과대표현을 수정해야 한다.
둘째 빈번하게 경고 서한을 받는 경우가 색소규정 위반. FDA는 미국 수입 화장품 라벨을 검토하여 표기된 색소가 관련 규정을 준수하고 있는지를 판단하는데, 라벨에 색소 표기가 없어도 제품을 실험실로 보내 색소가 첨가되어 있는지 확인하기도 한다. 미준수 시 추후에 수입이 거절되거나 수입금지 리스트에 올라갈 수 있다. 따라서 해당 색소 용도에 대한 승인 확인→배치 인증(Batch Certification)이 필요한 색소인지 확인→전성분 표기시 색소 이름이 FDA 표기 확인 등을 거치도록 한다.
셋째 미생물 오염 불량(adulterated cosmetic) 화장품은 불법이다. “라벨링에 규정된 사용 조건 또는 관습적이거나 일상적인 사용 조건에서 소비자에게 해로울 수 있는 독성 또는 유해 물질이 제품에 포함되어 있는 경우”에 불량 화장품으로 간주된다.
넷째 의료기기인데 화장품으로 판매한 경우도 경고 서한을 받게 된다. 마이크로 니들 제품이 혈관과 신경에 손상을 줄 가능성, 안전성 우려로 사전허가를 받아야 하는 제품이라며 경고를 받았다. 또 인허가를 받지 않는 필러나 하이드로겔 제품은 불량 화장품으로 간주된다.
다섯째 OTC Drug의 해외 제조소 실사에서 의약품 GMP 위반 사례도 있다. 이는 화장품 및 의약품 규정 위반에 해당된다. 또 경고서한 받은 제조소의 제품을 공급받는 경우도 경고를 받게 된다.
여섯째 “본 제품을 바른 후 열을 가하고 고데기를 하세요”라는 표시에서 라벨링의 사용법을 따를 때 독성 성분(포름알데히드)이 배출된다면 불량 화장품으로 간주되며 이는 안전성 및 라벨링 위반에 해당된다.
일곱째 FDA는 해외 제조소 실사를 하게 되는데 이때 의약품 GMP를 준수하지 않은 경우 경고서한을 받는 사례가 잦다. 특히 조직 및 작업원, 설비 세척 및 유지 관리, 컴퓨터 시스템의 인증된 직원만이 통제권 행사 등 매뉴얼 미준수 시 지적받게 된다.

FDA가 경고서한을 발행하는 이유는 실제 억류 및 반입 거부로 가기 전의 조치로 업체가 자발적으로 시정할 것을 기대하기 때문이다. 따라서 서한에서 정한 기한 내에 시정조치 결과를 통보해야 불이익을 방지할 수 있다.
미국 진출 시 제조사 등록은 필수이며 만일 미등록시 미국 내 제조·수출입·유통 모두 할 수 없다. 책임자로는 제조사, 포장업자, 유통업체 중 누구나 등록 가능하다. 시설등록비용에 대해 존권 대표는 “화장품의 경우 2년마다 갱신을 해야 한다고 나와 있어 2년마다 내야 할 것으로 예측하고 있다. 현재 FDA에서 MoCRA 관련 가이드라인, 비용, 시스템 구축 등 공식 발표 되면 업데이트 해드리겠다”고 전했다.
만약 FDA로부터 문제점(Warning Letter, OTC inspection fail, Import Alert)을 지적받은 경우에는 재검사 또는 시정조치를 해결한 후 등록해야 한다. 또 OTC제조와 달리 화장품 제조의 GMP 기준은 ISO 22716을 준수(미국 협회)하는 선에서 결정이 될 가능성이 있다고 존권 대표는 설명했다.






























